[Apostila online] - Tópico 2: Tamanho é Documento?
| Site: | Moodle USP: e-Disciplinas |
| Curso: | 05 - Zoologia |
| Livro: | [Apostila online] - Tópico 2: Tamanho é Documento? |
| Impresso por: | Usuário visitante |
| Data: | quinta-feira, 11 jul. 2024, 18:19 |
Descrição
[Apostila online] Tópico 2: Tamanho é Documento?
Índice
- 1. Início de Conversa
- 2. Mãos à obra
- 2.1. Etapa 1
- 2.2. Etapa 2
- 2.3. Etapa 3
- 2.4. Etapa 4
- 2.5. Etapa 5
- 2.6. Etapa 6
- 2.7. Etapa 7
- 3. Finalizando
- 4. Ampliando o Conhecimento
- 4.1. Quadro - Medindo o tamanho
- 4.2. Quadro - Escalas
- 4.3. Quadro - Representações esquemáticas em Biologia
- 5. Sugestão de Atividades
- 6. Bibliografia
- 7. Anexos
1. Início de Conversa
 Conforme a proposta seguida no tema diversidade de animais invertebrados, entende-se que o tipo de divulgação associado a estes organismos não determina sua importância real na natureza. Assim, estudar a diversidade deles deve ser levado em conta para a boa formação do biólogo. Espera-se que ele compartilhe tais informações, instruindo pessoas de outras áreas sobre as peculiaridades das micro, meio e mesofaunas, com possíveis aplicações médicas e econômicas, além de seu indiscutível papel ecológico no ambiente que residem. Sendo de grande valia também para apresentar a diversidade animal aos alunos do Ensino Médio, muito superior em número e qualidade do que imaginam.
Conforme a proposta seguida no tema diversidade de animais invertebrados, entende-se que o tipo de divulgação associado a estes organismos não determina sua importância real na natureza. Assim, estudar a diversidade deles deve ser levado em conta para a boa formação do biólogo. Espera-se que ele compartilhe tais informações, instruindo pessoas de outras áreas sobre as peculiaridades das micro, meio e mesofaunas, com possíveis aplicações médicas e econômicas, além de seu indiscutível papel ecológico no ambiente que residem. Sendo de grande valia também para apresentar a diversidade animal aos alunos do Ensino Médio, muito superior em número e qualidade do que imaginam.
Para contemplarmos um exemplo dessa diversidade relativamente, analisaremos a fauna que se encontra geralmente em reservatórios de água doce. Muitos seres vivos habitantes de corpos de água doce, desde grandes lagos de hidrelétricas e rios caudalosos até microambientes como as pequenas quantidades de água acumuladas em musgos e bromélias (denominados fitotelmata), representam diferentes grupos de animais e protistas. Não há filos animais exclusivos da água doce, sendo o mais comum encontrar umas tantas espécies habitando a água doce e os demais representantes do filo vivendo no mar ou no ambiente terrestre. Há ainda grupos que passam somente parte de seus ciclos de vida na água doce, passando a explorar habitats totalmente diversos na fase adulta; é o caso de muitos insetos e vermes. Assim, nós nos deparamos com uma diversidade acentuada de planos corporais e soluções diversas para a sobrevivência.
Quando ocorre a oportunidade de se encontrar um organismo, surgem perguntas biológicas básicas: como se chama (nome); onde mora (habitat); qual sua profissão (função ou papel que desempenha no local em que vive); seus hábitos (como se locomove, se alimenta, se reproduz, se defende); suas dimensões (tamanho relativo), entre outras questões. De posse de tais informações, passa-se a investigá-lo de acordo com o interesse do investigador.
Portanto, passar pela experiência de encontrar e reconhecer devidamente diferentes invertebrados torna-se uma atividade não apenas necessária, mas também enriquecedora. Vamos visualizar um vídeo sobre dois pequenos animais marinhos, pouco conhecidos, vivendo em associação?
Legenda: O copépode Sapphirina angusta, vive na cavidade do corpo do tunicado planctônico Thalia democratica, se alimentando dos tecidos do hospedeiro, o que pode causar sua morte.
Fonte: http://cifonauta.cebimar.usp.br
Se desejar fazer o download do video, clique aqui
No próximo tópico, “mãos à obra”, vamos realizar uma atividade envolvendo animais de corpos de água doce.
2. Mãos à obra
A tividades relacionadas à obtenção de organismos e sua posterior triagem visando à identificação exigem tanto concentração nas especificações da metodologia de coleta, descritas para cada grupo de interesse, como organização das informações referentes aos exemplares coletados. É imprescindível que dados referentes ao material sejam anotados nas etiquetas interna e externa do recipiente de armazenagem da amostra. No laboratório, equipamentos (instrumentos ópticos, por exemplo) são utilizados para possibilitar a visualização de detalhes que permitam a caracterização dos táxons encontrados.
tividades relacionadas à obtenção de organismos e sua posterior triagem visando à identificação exigem tanto concentração nas especificações da metodologia de coleta, descritas para cada grupo de interesse, como organização das informações referentes aos exemplares coletados. É imprescindível que dados referentes ao material sejam anotados nas etiquetas interna e externa do recipiente de armazenagem da amostra. No laboratório, equipamentos (instrumentos ópticos, por exemplo) são utilizados para possibilitar a visualização de detalhes que permitam a caracterização dos táxons encontrados.
A seguir, é apresentado um protocolo para coleta e cultivo de diversos invertebrados de água doce, proposto como fonte para consulta e aperfeiçoamento do conhecimento associado à diversidade de animais invertebrados de pequeno porte. O protocolo instrutivo compõe-se de 7 etapas sequenciais e todas podem ser cumpridas. Apenas a última etapa indica uma atividade que deve ser produzida após a leitura e/ou a experiência da coleta e cultivo dos animais conforme instruções dadas nas 6 etapas anteriores. O cursista não é obrigado a passar pela parte prática, muito menos sacrificar os animais envolvidos. Aqui são apresentadas técnicas científicas úteis ao trabalho em laboratórios de pesquisa. Pensando no curso do Ensino Médio e havendo possibilidade de coleta, após a visualização dos animais, eles podem ser devolvidos com vida ao ambiente onde foram coletados.
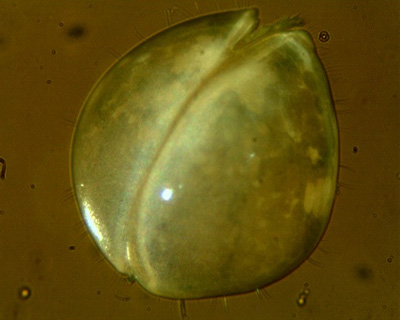 Figura 1. Animal residente em ambientes fitotelmáticos, como bromélias, por exemplo. Alimenta-se de detritos e possui glândulas serígenas para se deslocar com fios de seda nas folhas das bromélias. Trata-se de um crustáceo ostrácode, chamado Elpidium bromeliarum, facilmente encontrado em regiões mais conservadas de mata que possuam bromélias.
Figura 1. Animal residente em ambientes fitotelmáticos, como bromélias, por exemplo. Alimenta-se de detritos e possui glândulas serígenas para se deslocar com fios de seda nas folhas das bromélias. Trata-se de um crustáceo ostrácode, chamado Elpidium bromeliarum, facilmente encontrado em regiões mais conservadas de mata que possuam bromélias.
Fonte: Cortesia de Elise Vargas Pereira.
2.1. Etapa 1
| Etapa 1 |
|
Coleta e Cultivo de Invertebrados de Água Doce - I Objetivos:
Material de coleta e de laboratório necessários:
|
Assista ao vídeo da Profª Sônia Lopes e colaboradores sobre: Visualização de técnicas de cultivo de protistas.
2.2. Etapa 2
| Etapa 2 | |
|
Coleta e Cultivo de Invertebrados de Água Doce - II Procedimentos prévios: campo e laboratório
Figura 05: luvas para proteger as mãos durante as coletas. |
2.3. Etapa 3
| Etapa 3 |
|
Coleta e Cultivo de Invertebrados de Água Doce - III No laboratório: Triagem
Figura 6: A: colocando alíquota da amostragem com auxílio de pipeta, lâmina e lamínula. B: microscópio óptico com câmara clara para fazer desenhos. |
Assista ao vídeo Profª Sônia Lopes e colaboradores sobre: Visualização da diversidade de organismos em corpos de água doce.
Se desejar fazer o download do video, clique aqui
Conheça a galeria de fotos de espécimes que podem ser encontrados em amostras de água doce. Clique em um número da tabela e visualize os organismos que estão devidamente identificados (gêneros em itálico e outras categorias taxonômicas em caixa alta).
2.4. Etapa 4
| Etapa 4 |
|
Coleta e Cultivo de Invertebrados de Água Doce - IV No laboratório: Culturas: A. Preparação do meio:
Nota: dentro de três ou quatro dias, aparecerão fungos e bactérias concentrados principalmente ao redor dos grãos de arroz; eles servirão de alimento para os organismos em cultura. B. Montagem das culturas:
|
2.5. Etapa 5
| Etapa 5 |
|
Coleta e Cultivo de Invertebrados de Água Doce - V No laboratório: Culturas: C. Observação das culturas após uma semana ou mais:
Procedimento 1: Transfira uma gota da cultura contendo algum substrato para uma lâmina limpa e cubra a preparação com uma lamínula limpa. Observe ao microscópio. Procedimento 2: Transfira uma gota da cultura contendo algum substrato para uma lâmina limpa, deite sobre a gota uma malha bastante esgarçada de fiapos de algodão, e cubra a preparação com uma lamínula limpa. O objetivo da malha é aprisionar os organismos em áreas mais restritas, ao mesmo tempo em que oferece um suporte à lamínula da preparação e ajuda a evitar o esmagamento dos organismos mais espessos. O excesso do meio pode ser removido com tiras de papel de filtro ou guardanapo de papel. Observe ao microscópio. Para identificar os organismos, utilize a bibliografia indicada ou a galeria de fotos. Represente-os esquematicamente e anote o tipo de movimento que realizam e as particularidades que julgar importantes (ver procedimento no item Triagem, subitem 5). Manutenção das culturas: Mantenha as culturas em local abrigado do sol, de preferência cobertas com papel preto, folhas de jornal ou ainda em um armário fechado. Em cidades de clima frio, aqueça o local das culturas com aquecedor ou com uma ou mais luminárias com lâmpada de 25 W, mantidas acerca de 25 cm de altura em relação à bancada. Tais cuidados aumentarão as chances de as culturas perdurarem por meses e até por anos. Também é necessário que novos grãos de arroz sejam adicionados quando os existentes na cultura estiverem desaparecendo. A adição de mais água (gotejamento) será necessária para manter o nível do meio. Também é muito importante o cuidado de não se manipular substâncias venenosas, como formol e álcool, próximo ao local das culturas, ou introduzir na cultura pipetas e instrumentos já utilizados para manipular animais fixados ou produtos químicos.
|
2.6. Etapa 6
| Etapa 6 |
|
Coleta e Cultivo de Invertebrados de Água Doce - VI No laboratório: Culturas: Preparação de culturas puras: Em uma placa com meio preparado segundo procedimento descrito no item “Culturas – A. Preparação do meio”, inocule indivíduos do táxon desejado (p. ex., amebas, vermes, tardígrados etc.) utilizando uma pipeta nova e limpa para evitar a inoculação de organismos indesejados. A cultura de euglena ou paramécio deve ser feita inoculando-se os indivíduos em um frasco de 250 ml (tipo frasco de maionese) contendo água até a metade de sua capacidade e colocando-se 1/3 de uma folha fresca e lavada de alface. Novos pedaços de folha de alface devem ser adicionados quando aqueles colocados na cultura estiverem desaparecendo. Culturas de paramécio podem também ser obtidas substituindo-se a folha de alface fresca por folha de alface desidratada em estufa a 40 – 50oC. Para a desidratação das folhas, colocam-se folhas de alface lavadas entre folhas de papel toalha. A pilha de material assim preparada deve permanecer na estufa até as folhas se tornarem marrons. O processo leva 2 a 3 dias. Retire as folhas de papel toalha e as folhas de alface devem ser guardadas em recipiente com tampa. A vantagem é que se disporá de substrato alimentício para as culturas por um longo período de tempo. A experiência nos tem mostrado que as culturas de paramécio se desenvolvem melhor utilizando folhas desidratadas em vez de folhas frescas. Hidras podem ser mantidas no laboratório em aquários pequenos ou em outros recipientes. A água deve ser do local de coleta, filtrada em papel de filtro, ou água mineral. O local onde ficará o aquário deve ser iluminado e pode receber luz solar direta por algumas horas durante o período da manhã. Isto porque hidras verdes contêm simbiontes que realizam fotossíntese. Hidras são animais carnívoros e devem ser alimentadas adicionando-se zooplâncton à água. O ideal é manter no mesmo aquário/recipiente populações de microcrustáceos (copépodes, cladóceros e ostrácodes), que servirão de alimento para as hidras. Planárias são facilmente mantidas em recipientes com água do local de coleta, filtrada em papel de filtro, ou água mineral. São facilmente alimentadas com pequenas porções cruas de fígado de galinha ou boi. Uma porção de fígado de 1 a 2 cm de lado, amarrada a uma das extremidades de um pedaço de barbante (a outra extremidade ficará para fora do aquário) é deixada sobre o fundo ou encostada na parede do aquário. As planárias serão atraídas para o alimento, sobre o qual ficarão até estarem saciadas. Após umas duas horas, retirar o alimento restante para não estragar a água. Outro procedimento é trocar toda a água vertendo-a e colocando água nova. O risco de perda de algum animal é baixo, visto que os animais aderem às paredes do recipiente. Não remova bolinhas pretas que surgirem sobre as paredes do recipiente. Elas são casulos depositados pelas planárias, dos quais eclodirão jovens.
|
2.7. Etapa 7
| Etapa 7 |
|
Coleta e Cultivo de Invertebrados de Água Doce - VII Plano de Atividades Cada cursista deverá elaborar seu próprio plano ou protocolo de coleta e cultivo de invertebrados de água doce, adaptado aos seus alunos, que conterá: Título Objetivo(s) Duração (em horas-aula ou dias ou semanas) Coleta do material (onde e como) Manutenção do material no laboratório Procedimentos a serem desenvolvidos para atingir os objetivos propostos (execução da atividade) Bibliografia consultada (se houver). Será avaliada a criatividade, exequibilidade, clareza e objetividade na redação do plano e adequação à série escolhida para a aplicação do plano.
|
3. Finalizando
 A diversidade de metazoários e protistas microscópicos está longe de ser totalmente descrita, e fazer estimativas sobre essa variedade é um exercício sujeito a muitas críticas e poucas chances de comprovação científica. Realizar levantamentos faunísticos para aprimorar o conhecimento de determinado táxon se torna uma atividade importante, com vistas a oferecer ferramentas para se compreender seu papel no ambiente em que vive e a proposição de estratégias para sua conservação.
A diversidade de metazoários e protistas microscópicos está longe de ser totalmente descrita, e fazer estimativas sobre essa variedade é um exercício sujeito a muitas críticas e poucas chances de comprovação científica. Realizar levantamentos faunísticos para aprimorar o conhecimento de determinado táxon se torna uma atividade importante, com vistas a oferecer ferramentas para se compreender seu papel no ambiente em que vive e a proposição de estratégias para sua conservação.
A correta identificação e representação dos organismos é prioritária nesse processo de aprendizagem enfocando os invertebrados. A representação fidedigna de estruturas corporais, bem como de suas dimensões, possibilita, aos diferentes interessados no grupo taxonômico, discussões construtivas sobre sua biologia a partir das características morfológicas. Veja um exemplo nas imagens a seguir:

Figura 13: diferenças na morfologia em apêndices sexuais masculinos de ostracódes, servem para diferenciar espécies do gênero Elpidium, por exemplo. Os dois animais mediam cerca de 1 mm e foram removidos de suas conchas além de terem seus apêndices sexuais dissecados. A: Elpidium bromeliarum encontrado na região de Botuverá – SC (100x) e B: Elpidium sp.n. encontrado na região de Intervales – SP (100x). A espécie B é nova e está em processo de investigação, associando outros critérios de classificação além da morfologia evidenciada nas imagens acima.
Fonte: Cortesia de Elise Vargas Pereira.
4. Ampliando o Conhecimento
 Organismos diminutos, muitas vezes unicelulares, como os protistas que foram referidos como protozoários na literatura em voga até os anos 1960, são vistos como formas primitivas de vida. No entanto, vários deles atingem tamanho de alguns milímetros, sendo, portanto, visíveis a olho nu. Por outro lado, há grupos de metazoários que são menores que isso em tamanho, embora sejam pluricelulares. Assim, por exemplo, podemos encontrar diciemídeos (filo Dicyemida - Figura 1 e Figura 2) parasitas de cefalópodes (polvos e sépias), que possuem apenas cerca de 40 a 50 células corporais medindo cerca de 0,1mm, e também encontrar espécies de protistas que atingem 5mm, como algumas amebas (Amoeba proteus - Figura 3 e Figura 4). Portanto, torna-se fundamental representar o animal em um tamanho visível sem, contudo, perder a noção de seu real tamanho, preservando-a através de escalas métricas inseridas na representação do organismo estudado.
Organismos diminutos, muitas vezes unicelulares, como os protistas que foram referidos como protozoários na literatura em voga até os anos 1960, são vistos como formas primitivas de vida. No entanto, vários deles atingem tamanho de alguns milímetros, sendo, portanto, visíveis a olho nu. Por outro lado, há grupos de metazoários que são menores que isso em tamanho, embora sejam pluricelulares. Assim, por exemplo, podemos encontrar diciemídeos (filo Dicyemida - Figura 1 e Figura 2) parasitas de cefalópodes (polvos e sépias), que possuem apenas cerca de 40 a 50 células corporais medindo cerca de 0,1mm, e também encontrar espécies de protistas que atingem 5mm, como algumas amebas (Amoeba proteus - Figura 3 e Figura 4). Portanto, torna-se fundamental representar o animal em um tamanho visível sem, contudo, perder a noção de seu real tamanho, preservando-a através de escalas métricas inseridas na representação do organismo estudado.
Uma maneira simples de estimar o tamanho corporal de diferentes organismos é fazer uma medida relativa comparativa de ambos. Consulte o pdf “Protocolo Tamanho Corporal Relativo” (que também está disponível na abertura da semana 2), feito especialmente para que você possa utiliza-lo em aula prática com seus alunos do Ensino Médio.
Neste tópico serão fornecidos quadros com informações sobre tamanho, escalas e representações esquemáticas biológicas, que são muito úteis aos biólogos de forma geral, independentemente do ser vivo em que focam seu trabalho.
O cursista deve consultá-los para realizar uma atividade associada a este conteúdo mais à frente no tópico “sugestão de atividade”. Veja a imagem a seguir e pense como você faria para dimensionar adequadamente estes organismos! Com as dicas dos próximos quadros informativos você vai conseguir!

Figura 14: Radiolários de diferentes morfologias e tamanhos, aumentados 200x, e tratados com corante para facilitar a visualização dos mesmos.
Fonte: Thinkstock
4.1. Quadro - Medindo o tamanho
|
Medindo o Tamanho |
|
Às vezes, torna-se difícil saber o tamanho real de um organismo observado ao microscópio, principalmente quando não se tem disponível uma retícula micrometrada associada à lente objetiva como ponto de referência para medições. Uma solução para isso é medir o campo visual do menor aumento do microscópio, com o auxílio de uma régua milimetrada transparente de boa qualidade e, a partir daí, fazer inferências sobre o tamanho do organismo que está sendo visualizado. Para tanto, siga os passos abaixo:
|
4.2. Quadro - Escalas
|
Escalas |
|
Uma escala é um método de ordenação de grandezas físicas e químicas, qualitativas ou quantitativas, que permite uma dada comparação. Em desenhos esquemáticos, para representar o tamanho de um organismo ou de alguma estrutura de seu corpo, podemos utilizar uma escala numérica, que pode ser representada de maneira gráfica. A escala gráfica é representada sob a forma de um segmento de reta, normalmente subdividido em seções ao longo das quais são registradas as distâncias reais correspondentes às dimensões do segmento. A escala traduz assim a relação entre a distância no desenho e a correspondente distância na realidade, ou seja, indica quantas vezes a realidade foi reduzida ou aumentada. Em trabalhos de campo, é comum realizar o registro fotográfico de um organismo próximo a um objeto de tamanho conhecido para se ter uma idéia generalizada do tamanho do espécime de interesse. Assim, são utilizadas moedas, réguas milimetradas, a mão de uma pessoa, etc. Representações esquemáticas mais precisas indicam um segmento de reta que corresponda a uma unidade métrica (ex: 1mm). Com este referencial é possível saber quantos milímetros existem em uma dada representação de um organismo qualquer, verificando quantos desses segmentos de 1mm podem ser inseridos, um após o outro, no desenho correspondente. É possível fazer uma escala sob microscópio óptico, utilizando uma régua milimetrada como foi explicado no quadro informativo anterior sobre medida do tamanho. Também é possível comprar lâmina micrométrica com uma régua de tamanho diminuto, conhecida como gradícula, própria para observação ao microscópio óptico e estereomicroscópio. Observação: consultar site abaixo quando ocorrer dificuldade com conversões de medidas. http://www.webcalc.com.br/conversoes/comprimento.html Fonte(s): http://www.webcalc.com.br/
|
4.3. Quadro - Representações esquemáticas em Biologia
|
Representações esquemáticas em Biologia |
|
Procedimentos para a elaboração de um esquema ou desenho (adaptado de Boolootian & Heyneman, 1969):
|
5. Sugestão de Atividades
 As representações (esquemas, figuras) de organismos podem gerar fontes de erro, que se multiplicam ao serem reproduzidas se a escala não for cuidadosamente elaborada. Erros comuns de escala incluem ausência, incorreção, tamanho impróprio, representação ambígua, unidade métrica incomum etc.
As representações (esquemas, figuras) de organismos podem gerar fontes de erro, que se multiplicam ao serem reproduzidas se a escala não for cuidadosamente elaborada. Erros comuns de escala incluem ausência, incorreção, tamanho impróprio, representação ambígua, unidade métrica incomum etc.
Compare as figuras abaixo sobre um radiolário e responda:
Qual delas possui a escala mais adequada? Por quê?

6. Bibliografia
 BOOLOOTIAN & HEYNEMAN. An ilustrated laboratory text in zoology. 2 ed. Holt, R. e W. Inc. 1969.
BOOLOOTIAN & HEYNEMAN. An ilustrated laboratory text in zoology. 2 ed. Holt, R. e W. Inc. 1969.
KIHARA T. C. & ROCHA, C. E. F. Técnicas para estudo taxonômico de copépodes harpacticóides da meiofauna marinha. 1ed. Porto Alegre, RS: Asterisco, 2009.
RUPPERT, E. E.; FOX, R. & BARNES, R. D. Zoologia dos invertebrados. 7. ed. São Paulo: Roca, 2005.
STORER, T. J.; USINGER, R. L.; STEBBINS, R. C. & NYBAKKEN, J.W. Zoologia geral. 7. ed. São Paulo: Companhia Editora Nacional, 2000.
JAHN T. L. & JAHN F. F. How to know the protozoa. WM. C. Brown Co. Publishers. Dubuque, Iowa, 1949.
Sites:
7. Anexos
 Visualização de técnicas de cultivo de protistas:
Visualização de técnicas de cultivo de protistas:
http://wms.emm.usp.br:7070/ib/Cultivando_Microorganismos_multi.wmv
Visualização da diversidade de organismos em corpos de água doce:
http://wms.emm.usp.br:7070/ib/O_Mundo_Invisivel_da_Lagoa_multi.wmv
Visualização da diversas imagens e vídeos de organismos marinhos:




 Figura 04: recipiente de coleta.
Figura 04: recipiente de coleta.













